أفاد باحثون في كلية الطب في جامعة جونز هوبكنز بأنهم نجحوا في استخدام تقنية “الصدمة ثم التجميد” (zap-and-freeze) لرصد التواصل السريع بين الخلايا العصبية في نسيج حي مأخوذ من الفئران والبشر على حدٍّ سواء. وقد أتاح لهم هذا الأسلوب مراقبة التفاعلات التي تحدث عادة بسرعة تفوق قدرة التقنيات التقليدية على تتبّعها.
وبحسب الفريق البحثي، فإن النتائج المنشورة في ٢٤ تشرين الثاني/نوفمبر في مجلة Neuron، والمدعومة من المعاهد الوطنية للصحة الأميركية، قد تساعد في الكشف عن الأسباب البيولوجية الكامنة خلف الأشكال غير الوراثية من مرض باركنسون. وتشير مؤسسة باركنسون إلى أنّ الحالات العفوية (غير الوراثية) تمثل الغالبية العظمى من تشخيصات المرض. وتتميز هذه الحالات باضطرابات في المشبك العصبي، وهو موقع دقيق يقوم فيه عصبون واحد بتمرير الإشارة إلى آخر. ونظراً لصِغَر حجم هذا الموضع وسرعة حدوث التفاعلات فيه، فقد كان من الصعب دراسته بشكل مفصّل، وفق ما يوضحه شيغيكي واتانابي، الحاصل على الدكتوراه وأستاذ البيولوجيا الخلوية في طب جونز هوبكنز، والكاتب الرئيسي للدراسة.
ويقول واتانابي: “نأمل أن تساعدنا هذه التقنية الجديدة، التي تتيح تصوير ديناميكيات الغشاء المشبكي في أنسجة دماغية حيّة، على فهم أوجه التشابه والاختلاف بين الأشكال الوراثية وغير الوراثية من المرض”. كما يضيف أنّ هذه الطريقة قد تمهّد مستقبلاً لتطوير علاجات لهذا الاضطراب العصبي التنكّسي.
كيف تنقل المشابك العصبية الرسائل في الدماغ السليم
في الدماغ الصحي، تعمل الحويصلات المشبكية كحزم دقيقة تحمل الرسائل الكيميائية من عصبون إلى آخر. ويعدّ هذا التبادل أساسياً للتعلّم وتكوين الذاكرة ومعالجة المعلومات. ويشير واتانابي إلى أنّ فهم سلوك الحويصلات في الظروف الطبيعية هو المفتاح لتحديد نقاط الخلل التي يبدأ عندها التواصل العصبي بالتدهور في الأمراض العصبية.
وكان واتانابي قد ساهم سابقاً في ابتكار أسلوب “الصدمة ثم التجميد” لرصد التغيّرات السريعة في أغشية المشابك (ونُشرت نتائجه في عام ٢٠٢٠ في مجلة Nature Neuroscience). وتعتمد الطريقة على تحفيز نسيج دماغي بصدمة كهربائية قصيرة، يعقبها تجميد فوري للنسيج لحفظ البنية الخلوية بدقة بهدف فحصها لاحقاً بالمجهر الإلكتروني.
وفي دراسة أخرى نُشرت في Nature Neuroscience هذا العام، استخدم واتانابي التقنية نفسها على فئران معدّلة وراثياً للتحقيق في دور بروتين يُسمّى Intersectin. وقد أبرزت الدراسة كيف يساعد هذا البروتين في الحفاظ على الحويصلات المشبكية في موقع محدّد إلى حين جاهزيتها لإطلاق الرسائل وتنشيط العصبون المجاور.
اختبار التقنية على أنسجة من دماغ الإنسان
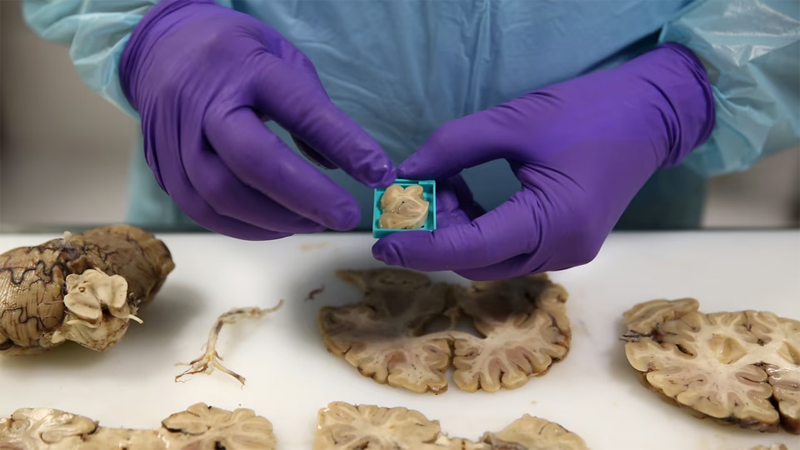
في هذه الدراسة الأحدث، فحص الفريق عينات من فئران سليمة وقارنها بأنسجة دماغية قشرية حيّة حصلوا عليها — بموافقة — من ستة أشخاص خضعوا لجراحة صرع في مستشفى جونز هوبكنز لإزالة آفات في الحُصَين. وبالتعاون مع ينز آيلرز وكريستينا ليبمان من جامعة لايبزيغ في ألمانيا، أكد الباحثون أولاً موثوقية تقنية “الصدمة ثم التجميد” في أنسجة الفئران عبر مراقبة إشارات الكالسيوم التي تُعدّ الشرارة التي تدفع العصبونات لإطلاق النواقل العصبية.
بعد ذلك، حفّزوا خلايا عصبية في الفئران باستخدام التقنية نفسها ورصدوا اللحظة الدقيقة التي تندمج فيها الحويصلات المشبكية مع الغشاء الخلوي لإطلاق رسائلها الكيميائية، كما وثّقوا عملية استرجاع الخلايا لهذه الحويصلات وإعادة تدويرها لاحقاً، وهي العملية المعروفة باسم الادخال الخلوي (Endocytosis).
وعندما طبّق الفريق التقنية نفسها على أنسجة دماغية بشرية، وجدوا الخطوات ذاتها لآلية تدوير الحويصلات تجري بشكل مطابق داخل الخلايا العصبية البشرية.
اكتشاف بروتين أساسي في دماغي الإنسان والفأر
في كلا النوعين، حدّد الباحثون وجود بروتين Dynamin1xA، الضروري لعملية إعادة تدوير الغشاء المشبكي بسرعة فائقة، في المواقع التي يُعتقد أنّ الإدخال الخلوي يحدث فيها. وتشير هذه النتيجة إلى أنّ الآليات الجزيئية التي لوحظت في الفئران تعكس بدقة ما يجري في الدماغ البشري.
ويقول واتانابي: “تشير نتائجنا إلى أن الآلية الجزيئية لعملية الإدخال الفائق السرعة محفوظة بين الفئران وأنسجة الدماغ البشرية”، لافتاً إلى أنّ هذا يعزّز قيمة استخدام نماذج الفئران لدراسة بيولوجيا الدماغ البشري.
وينظر واتانابي إلى المستقبل بأمل في تطبيق تقنية “الصدمة ثم التجميد” على أنسجة دماغية تُجمع — بموافقة — من مرضى باركنسون الخاضعين لإجراءات تحفيز الدماغ العميق، بهدف رصد كيف قد تختلف ديناميكيات الحويصلات في العصبونات المتأثرة بالمرض.
التمويل والمساهمون
حصلت الدراسة على تمويل من المعاهد الوطنية للصحة (U19 AG072643, 1DP2 NS111133-01, 1R01 NS105810-01A1, R35 NS132153, S10RR026445)، ومؤسسة هوارد هيوز الطبية، ومؤسسة كازاتو، والجمعية الأميركية اللبنانية السورية للأعمال الخيرية (ALSAC)، ومعهد الأحياء البحرية، وجامعة لايبزيغ، ومؤسسة رولاند إرنست، وطب جونز هوبكنز، ومبادرة تشان زوكربيرغ، ومؤسسة أبحاث الدماغ، ومؤسسة هيليس، ومؤسسة روبرت وج. هيلين كليبرغ، ومؤسسة ماكنايت، وصندوق إستر أ. وجوزف كلينغنستاين، ومؤسسة فالي.
وشملت المساهمات البحثية كلاً من: تشيلسي إدينغز، مينغوا فان، يوتا إيموتو، كي إيتو، شيامارا ماكدونالد، ويليام أندرسون، بول ورلي، وديفيد ناوين من جونز هوبكنز، إلى جانب ينز آيلرز وكريستينا ليبمان من جامعة لايبزيغ.
المصدر:
المواد العلمية المقدّمة من كلية الطب في جامعة جونز هوبكنز.


